Метанол газовым промыслам!
Содержание:
- Токсичность
- Лечение и профилактика
- Режимные параметры процесса синтеза метанола
- Оказание неотложной помощи при отравлении метанолом
- Вхождение
- Получение предельных одноатомных спиртов
- Спецификации качества и анализ
- викторина
- Технологические схемы производства метанола
- Для чего нужен метанол?
- Картина Отравления:
- варианты
- НАРКОТИК ИЛИ ПИЩЕВОЙ ПРОДУКТ?
Токсичность
Употребление всего 10 мл чистого метанола может вызвать необратимую слепоту из-за разрушения зрительного нерва . 30 мл (1,0 жидких унций США) потенциально смертельны. Средняя смертельная доза составляет 100 мл (3,4 жидких унций США), то есть 1-2 мл / кг массы тела чистого метанола. Контрольная доза метанола составляет 0,5 мг / кг в сутки. Токсические эффекты начинаются через несколько часов после приема внутрь, и антидоты часто могут предотвратить необратимое повреждение. Из-за его сходства как по внешнему виду, так и по запаху с этанолом (алкоголь в напитках) трудно провести различие между ними; так же обстоит дело с денатурированным спиртом , фальсифицированными ликерами или алкогольными напитками очень низкого качества.
Метанол токсичен по двум причинам. Во-первых, метанол может быть фатальным из-за воздействия на центральную нервную систему, действуя как депрессант центральной нервной системы так же, как . Во-вторых, в процессе отравления он метаболизируется до муравьиной кислоты (которая присутствует в виде формиат-иона) через формальдегид в процессе, инициированном ферментом алкогольдегидрогеназой в печени . Метанол превращается в формальдегид через алкогольдегидрогеназу (ADH), а формальдегид превращается в муравьиную кислоту (формиат) через альдегиддегидрогеназу (ALDH). Преобразование в формиат с помощью ALDH происходит полностью, без обнаруживаемого формальдегида. Формиат токсичен, потому что он ингибирует митохондриальную цитохром-с-оксидазу , вызывая гипоксию на клеточном уровне и метаболический ацидоз среди множества других метаболических нарушений.
Вспышки отравления метанолом произошли в первую очередь из-за заражения употребляемого алкоголя . Это чаще встречается в развивающихся странах . Тем не менее, в 2013 году в США было зарегистрировано более 1700 случаев. Пострадавшие чаще всего взрослые мужчины. При раннем лечении результаты могут быть хорошими. Токсичность по отношению к метанолу была описана еще в 1856 году.
Из-за своих токсичных свойств метанол часто используется в качестве денатурирующей добавки для этанола, производимого для промышленного использования. Это добавление метанола освобождает промышленный этанол (широко известный как « денатурированный спирт » или «метилированный спирт») от акцизного налогообложения спиртных напитков в США и некоторых других странах.
В ходе COVID-19 пандемии , то за продуктами и лекарствами США обнаружили ряд дезинфицирующее продуктов , продаваемых , которые были помечены как содержащие этанол , но имели положительную реакцию на загрязнение метанола. Из-за токсического воздействия метанола при всасывании через кожу или проглатывании, в отличие от относительно более безопасного этанола, FDA распорядилось отозвать такие дезинфицирующие средства для рук, содержащие метанол, и выпустило предупреждение об импорте, чтобы предотвратить незаконный выход этих продуктов на рынок США. .
Лечение и профилактика
Обширность вредного воздействия еще раз доказывает потребность в немедленном обращении в медицинское учреждение. Именно медработник объяснит, что делать после отравления метиловым спиртом до прибытия скорой помощи и для предотвращения повторных эпизодов.
Лечение возможно только в стационаре. Специалистами проводится комплексное обследование и по итогам назначаются лекарственные препараты и мероприятия.
Применение соды, растворенной в воде, нейтрализует ожоги и снижает кислотность желудочной среды.
Этиловый спирт – признанный антидот для метилового. Он предотвращает образование продуктов распада.
Токсические отеки мозга, легких, возникающие в результате накопления жидкости в клетках, устраняют при помощи мочегонных средств, ускоряющих образование мочи и выводящих лишнюю воду. Предварительно у больного снимают приступы дрожи и судорог, обеспечивают состояние покоя.
Гемодиализ приводит в норму водный и электролитный баланс, очищает кровь от токсинов. Во время диализа рекомендуется поддерживать уровень этанола, так как он тоже выводится.
Офтальмологические лекарственные средства способствуют восстановлению зрительного нерва и сетчатки глаз.
Витамины восполняют потерю полезных веществ после проведенных процедур и ускоряют реабилитацию.
Своевременное медицинское вмешательство не гарантирует полного выздоровления. Последствия отравления могут быть необратимыми. Часто осложнениями оказываются задеты органы зрения, наблюдаются нарушения функций печени и пищеварения, нервные расстройства.
Нередки смертельные исходы. Известны случаи массового отравления с многочисленными жертвами, основанные на стремлении удешевить опьянение, но чужой горький опыт быстро забывается. Количество отравившихся растет. Лучший способ не оказаться в числе пострадавших – соблюдать профилактические меры безопасности.
Профилактика отравления метанолом предполагает:
- информирование населения о тяжелых последствиях использования технического спирта;
- подробное инструктирование работников, применяющих метанол;
- жесткий контроль хранения и расходования метилового спирта;
- проветривание рабочих помещений;
- обеспечение защитных средств;
- обязательные ежегодные медосмотры;
- запрещение использования метанола в бытовых условиях, замена нетоксичными средствами;
- проверка качества алкоголя и борьба с контрафактной продукцией.
Режимные параметры процесса синтеза метанола
Зависимость выхода метанола от температуры не линейна и
имеет выраженный максимум. Кривая зависимости количества образовавшегося
метанола от температуры проходит через экстремум при всех составах газа, причем
максимальный выход метанола наблюдается при 255–270 °С.
Интервал оптимальных температур, соответствующих наибольшему
выходу продукта, определяется активностью катализатора, объемной скоростью
газовой смеси и давлением. Процессы низкого давления (5–10 МПа) на
медьсодержащих катализаторах осуществляют при температурах 220–280 °С. Для
цинк-хромового катализатора характерны более высокие давления (20–30 МПа) и
температуры (350–400 °С).
Максимальное давление, применяемое в промышленных синтезах,
составляет 40 МПа; выше этого давления ускоряются побочные реакции и, кроме
того, увеличение затрат на компрессию газа ухудшает экономические показатели процесса.
В синтезах низкого давления повышение давления ограничено термической
стабильностью медных катализаторов.
С возрастанием объемной скорости газа выход метанола падает.
Это справедливо для синтеза как при высоком, так и при низком давлении. Такая
закономерность основана на том, что с увеличением объемной скорости уменьшается
время контакта газа с катализатором и, следовательно, концентрация метанола в
газе, выходящем из реактора .
Состав газовой смеси существенно влияет на степень
превращения сырья и производительность катализатора. В промышленных условиях
всегда работают с некоторым избытком водорода; максимальная производительность
наблюдается при молярном отношении Н2:СО = 4, на практике поддерживают отношение
2,15–2,25.
Оказание неотложной помощи при отравлении метанолом
Первым делом следует незамедлительно вызвать врача. Непредсказуемость реакции органов на отравление требует квалифицированной медицинской помощи.
Первая помощь при отравлении метиловым спиртом заключается в предельно быстром освобождении организма от токсина. Без постановки диагноза самостоятельно допускается провести промывание желудка теплым раствором пищевой соды, обеспечить обильное (8-12 л) питье, тепло и приток свежего воздуха.
Бессознательное состояние пострадавшего исключает проведение подобных процедур. Если не прощупывается пульс и отсутствует дыхание, нужно осуществить реанимационные мероприятия. Затем необходимо уложить человека на бок, укутать теплым покрывалом и дождаться приезда медиков.
Безусловная уверенность в том, что причиной отравления стал технический спирт, допускает использовать этиловый спирт как антитоксин. Раствор вводится внутривенно или путем проглатывания (1 мл чистого вещества на 1 кг массы человека) и препятствует реакции окисления. Следует знать, что похожие симптомы проявляются при алкогольной интоксикации в результате передозировки этилового спирта. В этом случае, дополнительная доза этанола может быть не спасительной, а смертельной. Применение любых препаратов без назначения медиков очень опасно.

Вхождение
Небольшие количества метанола присутствуют у нормальных здоровых людей. Одно исследование показало, что средний показатель выдыхаемого воздуха у испытуемых составляет 4,5 промилле . Среднее значение эндогенного метанола у людей 0,45 г / день может метаболизироваться из пектина, обнаруженного во фруктах; из одного килограмма яблока получается до 1,4 г метанола.
Метанол вырабатывается анаэробными бактериями и фитопланктоном .
Межзвездная среда
Метанол также содержится в больших количествах в областях звездообразования в космосе и используется в астрономии в качестве маркера для таких регионов. Он обнаруживается по его спектральным эмиссионным линиям.
В 2006 году астрономы с помощью радиотелескопов MERLIN в обсерватории Джодрелл-Бэнк обнаружили в космосе большое облако метанола размером 288 миллиардов миль (463 миллиарда км) в поперечнике. В 2016 году с помощью радиотелескопа ALMA астрономы обнаружили метанол в диске, формирующем планету, вокруг молодой звезды TW Hydrae .
Получение предельных одноатомных спиртов
К наиболее часто используемым химическим способам получения спиртов относятся:
1.Гидратация алкенов (промышленный способ получения этанола для технических целей)
(t, Р, кислая среда (катализатор))
2.Щелочной гидролиз галогеналканов (лабораторный способ получения)
(водный раствор щелочи, t)
3.Восстановление альдегидов и кетонов (лабораторный способ получения)
(t, катализатор –Ni)
Особые способы получения метанола и этанола
1.Получение метанола из синтез-газа (водяной газ, генераторный газ)
(t, Р, оксидные катализаторы)
2.Получение этанола ферментативным брожением глюкозы (получение этилового спирта для пищевых и медицинских целей)
(ферменты — дрожжи)
1. Гидратация алкенов
Гидратация алкенов используется в промышленности для получения спиртов из продуктов нефтепереработки.
Присоединение воды к алкенам происходит в присутствии разбавленной серной или фосфорной кислот. Эта реакция протекает в соответствии с правилом Марковникова, поэтому первичный спирт можно получить только из этилена, а остальные алкены дают вторичные или третичные спирты: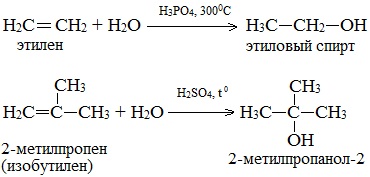
Этот метод в лабораторных условиях нашел ограниченную область применения для получения третичных спиртов.
2. Гидролиз галогеналканов в водном растворе щелочи
В лабораторных условиях спирты получают действием водного раствора щелочи на алкилгалогениды при нагревании, при этом атом галогена в галогеналкане замещается группой –ОН:
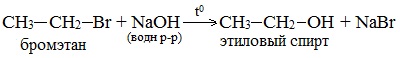
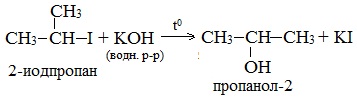
С помощью этой реакции можно получать первичные, вторичные и третичные спирты.
При действии спиртового раствора щелочи на галогеналканы происходит отщепление галогеноводорода и образование алкена.
3. Восстановление карбонильных соединений (альдегидов и кетонов)
Дегидрирование спиртов по своей химической сущности является окислением. Обратная реакция – гидрирование альдегидов, кетонов и эфиров карбоновых кислот – является, таким образом, их восстановлением.
При действии водорода в присутствии катализаторов (Ni, Pt, Pd) альдегиды восстанавливаются до первичных спиртов, а кетоны – до вторичных спиртов: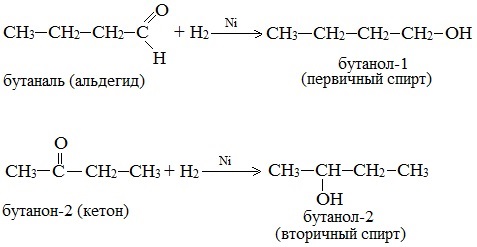
4. Восстановление эфиров карбоновых кислот
Гидрирование сложных эфиров проходит через стадию образования альдегидов:
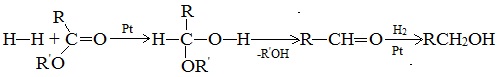
Этим методом в промышленности из метиловых эфиров высших кислот получают высшие первичные спирты, например:
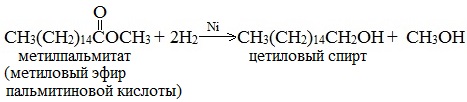
5. Гидролиз сложных эфиров карбоновых кислот в щелочной среде
Гидролиз сложных эфиров карбоновых кислот протекает как в кислой, так и в щелочной среде (водные или спиртовые растворы NaOH, КОН, а также Ba (OH)2, Ca (OH)2, Ba (OH)2, Ca (OH)2). Однако к образованию спиртов приводит гидролиз, протекающий необратимо в щелочной среде:
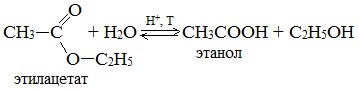
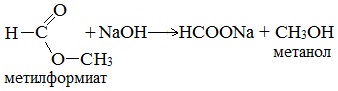
6. Синтез спиртов из карбонильных соединений с помощью магнийорганических соединений
Спирты образуются при многочисленных реакциях металлоорганических соединений с различными соединениями, содержащими карбонильную группу >С=О. Этим способом можно получать как первичные спирты, так и вторичные и третичные:
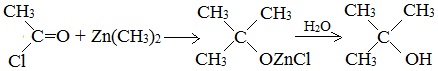
7. Окисление алканов
При мягком окислении метана кислородом воздуха в присутствии различных катализаторов образуются метанол, формальдегид или муравьиная кислота:
Специфические способы получения метанола и этанола
Производство метанола крупнотоннажное, т.к. метиловый спирт является исходным веществом для получения других продуктов органического синтеза.
В промышленности
1. Получение метанола из синтез-газа (водяной газ, генераторный газ)
а) Конверсия природного газа в синтез-газ
Его получают из метана с перегретым водяным паром:
б) Каталитический синтез метанола из оксида углерода (II) и водорода
В качестве катализаторов используют смесь оксидов цинка, меди и хрома, температуру поддерживают в интервале 200-300 оС, а давление – от 40 до 150 атм.
Газ на выходе из реактора содержит 3-5% CH3OH, затем газ охлаждают и конденсируют полученный метанол, а оставшийся газ смешивают с исходным газом и направляют снова в реактор.
Ранее метанол получали сухой перегонкой древесины без доступа воздуха (отсюда его название «древесный спирт»).
2. Получение этанола спиртовым брожением глюкозы
Ферментативный гидролиз крахмала – наиболее древний синтетический процесс, используемый человеком – до сих пор имеет огромное значение для получения этилового спирта.
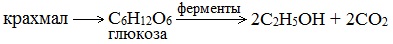
Протекает только в присутствии ферментов, которые вырабатывают некоторые микроорганизмы, например, дрожжи:
Глюкоза содержится во фруктовых соках. Глюкозу можно получить гидролизом крахмала (зерно, картофель, целлюлозные опилки):
Рубрики: Спирты Теги: Спирты
Спецификации качества и анализ
Метанол коммерчески доступен с различной степенью чистоты. Коммерческий метанол обычно классифицируется в соответствии со степенью чистоты A и AA ASTM. Чистота как класса A, так и степени чистоты AA составляет 99,85% по весу метанола. Метанол марки «AA» также содержит следовые количества этанола.
Метанол для химического использования обычно соответствует классу AA. Помимо воды, типичные примеси включают ацетон и этанол (которые очень трудно отделить перегонкой). УФ-видимая спектроскопия — удобный метод обнаружения ароматических примесей. Содержание воды можно определить титрованием по Карлу-Фишеру .
викторина
1. Что означает «мет» в «метаноле»?A. «Мет» означает, что химическое вещество имеет один атом углерода, так же, как «мет» в «метане».B. «Мет» означает, что вещество вызывает привыкание, подобно «мет» в «метамфетамине».C. «Мет» означает, что вещество является спиртом.D. Ни один из вышеперечисленных.
Ответ на вопрос № 1
верно. «Мет» в метаноле говорит вам, что у этого химического вещества есть один атом углерода, а достаточный «-анол» говорит вам, что это спирт. «Метанол» – это спирт с одним атомом углерода.
2. Что из перечисленного НЕ опасно для метанола?A. Он высокотоксичен при употреблении.B. Это очень огнеопасно.C. Он производит густой туманный пар, который может затенить ваше зрение.D. Ни один из вышеперечисленных.
Ответ на вопрос № 2
С верно. Метанол очень токсичен и легко воспламеняется. Однако затенение вашего зрения не является риском. Это невидимый газ и прозрачная жидкость. Это может на самом деле сделать метанол более опасным, так как он остается почти невидимым, даже когда он в огне.
3. Что бы вы ожидали, если бы вы реагировали на диоксид углерода с газообразным водородом и медным катализатором?A. Метанол будет создан без других побочных продуктов.B. Метанол будет создан с водой в качестве побочного продукта.C. Метанол будет создан с формальдегидом в качестве побочного продукта.D. Ни один из вышеперечисленных.
Ответ на вопрос № 3
В верно. В реакции CO2 с газом H2 метанол создается из углерода + водорода + один атом кислорода, а вода – из оставшегося кислорода и водорода.
Технологические схемы производства метанола
Технологический процесс получения метанола из оксида
углерода и водорода включает ряд операций, обязательных для любой технологической
схемы синтеза. Газ предварительно очищается от карбонила железа, сернистых соединений,
подогревается до температуры начала реакции и поступает в реактор синтеза метанола.
По выходе из зоны катализа из газов выделяется образовавшийся метанол, что
достигается охлаждением смеси, которая затем сжимается до давления синтеза и возвращается
в процесс.
Технологические схемы различаются аппаратурным оформлением главным
образом стадии синтеза, включающей основной аппарат колонну синтеза и теплообменник
.
На рисунке 1.2 представлена схема агрегата синтеза метанола
под давлением 5.5 МПа
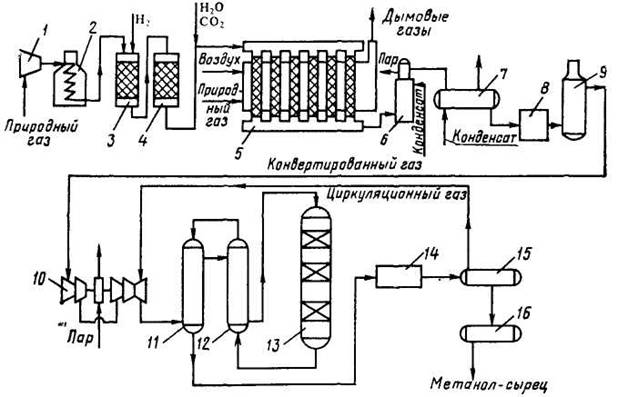 Схема производства метанола при давлении 5 МПа
Схема производства метанола при давлении 5 МПа
1, 10 – турбокомпрессоры; 2 – подогреватель природного газа; 3 – реактор гидрирования сернистых соединений; 4 – адсорбер; 5 – трубчатый конвертор; 6 – котел-утилизатор; 7, 11, 12 – теплообменники; 8, 14 – холодильники (АВО); 9, 15 – сепараторы; 13 – колонна синтеза; 16 – сборник
Природный газ сжимается турбокомпрессором 1 до давления 3
МПа, подогревается в подогревателе 2 за счет сжигания в межтрубном пространстве
природного газа и направляется на сероочистку в аппараты 3 и 4, где последовательно
осуществляется каталитическое гидрирование органических соединений серы и
поглощение образующегося сероводорода адсорбентом на основе оксида цинка.
После этого газ смешивается с водяным паром и диоксидом углерода в соотношении
СН4 : Н2О : СО2 = 1 : 3,3 : 0,24. Смесь
направляют в трубчатый конвертор 5, где на никелевом катализаторе происходит
пароуглекислотная конверсия при 850-870 °С. Теплоту, необходимую для конверсии,
получают в результате сжигания природного газа в специальных горелках.
Конвертированный газ поступает в котел-утилизатор 6, где
охлаждается до 280–290 °С. Затем теплоту газа используют в теплообменнике 7 для
подогрева питательной воды, направляемой в котел-утилизатор. Пройдя воздушный
холодильник 8 и сепаратор 9, газ охлаждается до 35-40 °С.
Охлажденный конвертированный газ сжимают до 5 МПа в компрессоре
10, смешивают с циркуляционным газом и подают в теплообменники 11, 12, где он
нагревается до 220–230 °С.
Нагретая газовая смесь поступает в колонну синтеза 13, температурный
режим в которой регулируют с помощью холодных байпасов. Теплоту реакционной смеси
используют в теплообменниках 11, 12 для подогрева поступающего в колонну газа.
Далее газовая смесь охлаждается в холодильнике-конденсаторе
14, сконденсировавшийся метанол-сырец отделяется в сепараторе 15 и поступает в
сборник 16. Циркуляционный газ возвращают на синтез, продувочные и танковые
газы передают на сжигание в трубчатую печь.
Вследствие снижения температуры синтеза при низком давлении
процесс осуществляется в условиях, близких к равновесию, что позволяет
увеличить производительность агрегата.
Принимаем для проектирования технологическую схему синтеза
метанола при низком давлении (5,5 МПа).
- Производство метанола под давлением 5 МПа
- Конструкция колонны синтеза метанола под давлением 5 МПа
Для чего нужен метанол?
Метанол имеет множество промышленных и научных целей.
Одним из наиболее распространенных видов использования метанола является ингредиент формальдегида. Этот химикат, который может быть получен из метанола, широко используется в производстве пластмасс, в том числе используемых в строительных материалах, автомобильных деталях, красках, взрывчатых веществах и искусственных тканях, устойчивых к морщинам. Формальдегид также используется гробовщиками и учеными для сохранения трупов и лабораторных образцов.
Метанол может быть использован для приготовления других полезных растворителей, включая уксусная кислота, диметиловый эфир и пропилен, который используется в антифризе. Метанол сам по себе также может быть ингредиентом антифриза.
Топливо как для бензиновых, так и для биодизельных автомобилей может включать метанол. Его легковоспламеняющаяся природа и полезность в качестве растворителя позволяют ему помочь другим видам топлива смешиваться и воспламеняться.
Чистый метанол даже использовался в качестве топлива для гоночных автомобилей. Это производит высокие скорости – но также привело к разрушительному пожару, который убил двух американских автогонщиков.
Метанольные пожары особенно опасны, потому что их очень легко зажечь, а пламя практически не видно. Это позволяет пожарам выходить из-под контроля и очень быстро ловить другие материалы.
Сегодня и в Соединенных Штатах, и в Европе действуют правила безопасности относительно того, сколько метанольного автомобильного топлива разрешено содержать.
Картина Отравления:
Чувствительность к М. С. даже у одного и того же человека очень непостоянна; Симптомы отравления (тошнота, рвота) могут наступить как вскоре после приема яда, так и через несколько часов, на следующий день или еще позднее. Между выраженностью первых явлений и исходом отравления обычно связи нет. В тяжелых случаях наблюдаются резкая синюха, глубокое и затрудненное дыхание, судороги, слабый учащенный пульс, отсутствие реакции зрачков. Смерть наступает от остановки дыхания. Пострадавшие, находящиеся в сознании, жалуются на головную боль, сильнейшие боли во всем теле, в желудке, мелькание перед глазами, неясность видения. Часто временно наступает улучшение, за которым следует новое и окончательное ухудшение.
Неисчезающее расширение зрачков указывает на возможность рецидива или стойких расстройств зрения.
Ингаляционные отравления парами редки, обычно вдыханию высоких концентраций М. С препятствует вызываемое им раздражение дыхательных путей и конъюнктивы.
Ранние симптомы хронического отравления: концентрическое сужение границ цветного зрения, нарастающее со стажем, изменения электрорети-нограммы, бледность или атрофия зрительного нерва, отек, сужение артерий и расширение вен сетчатки, гиперемия сосудистой оболочки глаза. Ослаблена реакция зрачков на свет. В крови — тромбопения; изменение уровня холестерина (Гринштейн). Субъективно: быстрая утомляемость, гоповная боль во второй половине дня, раздражительность, плаксивость, боль в правом подреберье.
При малых концентрациях отравление развивается постепенно и характеризуется . раздражением слизистых оболочек, частыми заболеваниями дыхательных путей» головными болями, звоном в ушах, невритами и расстройствами зрения.
Отравления при попадании на кожу обычно происходят при одновременном вдыхании паров. Описан случай отравления маляра, пролившего М. С. на ноги (промочил одежду и сапоги) и продолжавшего работать в этой одежде. Ослеп через несколько дней.
Действие на кожу: Чистый М. С. действует слабо; неочищенный древесный спирт раздражает кожу из-за наличия в нем примесей непредельных спиртов» альдегидов и т. д.
варианты
Интенсивно исследуются процессы, в которых метан окисляется непосредственно до метанола без обхода синтез-газа. Такой процесс устранит дорогостоящую стадию парового риформинга. Поскольку метильная группа в метаноле окисляется легче, чем в метане, селективное окисление затруднено при высоких конверсиях. Были исследованы катализаторы на основе смешанных оксидов металлов, например, на основе молибдена и висмута. Чтобы избежать дальнейшего окисления, используют чистый кислород при большом избытке метана. Проведенные до сих пор эксперименты показывают, что прямое окисление метана до метанола происходит по механизму Марса-ван-Кревелена через решеточный кислород. Однако достигаемая селективность и конверсия все еще слишком низки для экономичного осуществления процесса.
Другой возможный способ — прямая этерификация полученного метанола сильными кислотами. Сложные эфиры менее чувствительны к дальнейшему окислению. Метанол высвобождается на следующей стадии путем омыления . Эксперименты с солями платины, кобальта, палладия, меди и ртути в качестве катализаторов в серной или трифторуксусной кислоте были успешными, но с низкой конверсией. Обработка сложных эфиров оказалась неэкономичной; ни один процесс еще не был разработан для коммерческого использования.
Метанол можно получить из метана с помощью метанмонооксигеназы с использованием ферментативного катализа . Метанотрофные бактерии , такие как Methylococcus capsulatus , используют эту реакцию в качестве источника энергии, когда метан является единственным источником пищи. Масштабная реализация этого пути реакции в настоящее время не исследуется.
Химик и лауреат Нобелевской премии Джордж Олах разработал процесс, согласно которому метанол получают из диоксида углерода и воды путем подачи электрического тока в обратном направлении реакции, происходящей в топливных элементах; это позволяет «рециркулировать» CO 2 . Текущая проблема заключается в достижении необходимых высоких плотностей тока для крупномасштабного производства.
Перспективным представляется дальнейшее развитие известных процессов синтеза газа и метанола. Японские ученые разработали катализатор с конверсией двуокиси углерода и водорода в метанол с конверсией в два-три раза выше, чем у обычных катализаторов. Для этого процесса требуется дешевый водород, например Б. путем электролиза воды с использованием в идеале климатически нейтральной электроэнергии из возобновляемых источников энергии, возможно ядерной энергии, или в долгосрочной перспективе, возможно, энергии термоядерного синтеза, генерирующей электричество. Биотехнические или фотокаталитические процессы для производства водорода, а также цикл серная кислота-йод в сочетании с технологическим теплом (например, из высокотемпературных ядерных реакторов, таких как реактор с двумя жидкостями ) можно представить в качестве будущих перспектив.
НАРКОТИК ИЛИ ПИЩЕВОЙ ПРОДУКТ?
Наиболее авторитетным (но почему-то малоизвестным даже среди интеллигенции) является мнение по этому поводу Всемирной Организации Здравоохранения:
|
СПЕЦИАЛЬНОЕ РЕШЕНИЕ 28 сессии Всемирной Организации Здравоохранения (1975 год) АЛКОГОЛЬ — НАРКОТИК, ПОДРЫВАЮЩИЙ ЗДОРОВЬЕ НАСЕЛЕНИЯ |
|---|
Разумеется, это заключение не было научным открытием: оно опубликовано лишь как официальное подтверждение давно известного в науке факта. Медицина уже 300 лет диагностирует алкоголь как наркотический нейротропный и протоплазматический яд, то есть яд, воздействующий на нервную систему и все органы человеческого организма, разрушающий их структуру на клеточном и молекулярном уровнях.
В «Большой советской энциклопедии» (том 2, стр. 116) также чётко обозначено: «этанол относится к наркотическим ядам». «Санитарно-гигиенические нормы и правила» от 1999 года характеризуют алкоголь как «вещество с доказанной для человека канцерогенностью ».
Однако до сих пор находятся так называемые «учёные», которые продолжают упорно доказывать всем, что алкоголь — это «пищевой», да ещё и «очень полезный» продукт. Многие из них искренне заблуждаются, кому-то за это неплохо платят. Но в любом случае они дезориентируют общество, приучая легкомысленно относиться к наркотическому яду. Вместо того чтобы поставить вопрос о полном исключении этанола из пищевой промышленности и о защите населения от алкогольной эпидемии, эти «учёные» упрямо и бездоказательно настаивают на своей ошибочной и вредной установке.
Правда, алкоголь принято считать «специфическим» пищевым продуктом: на него наклеивают специальные акцизные марки; его почему-то не рекомендуют давать детям и беременным женщинам…
Но, несмотря на все эти «меры предосторожности», теперь уже не только больницы, но и все кладбища переполнены жертвами этого «продукта». А подавляющее большинство сидящих в тюрьмах совершили преступления именно под его «специфическим» воздействием.. Ещё в 1910 году Всероссийский съезд по борьбе с пьянством и алкоголизмом, на котором собралось 150 врачей и учёных медиков, специально рассматривал этот вопрос
В результате вынесено специальное решение:
Ещё в 1910 году Всероссийский съезд по борьбе с пьянством и алкоголизмом, на котором собралось 150 врачей и учёных медиков, специально рассматривал этот вопрос. В результате вынесено специальное решение:
|
Пищевым продуктом может быть только такое вещество, которое является абсолютно безвредным для организма. Алкоголь же как наркотический яд в любых дозах наносит человеку огромный вред: отравляя и разрушая организм, он сокращает жизнь человека в среднем на 20 лет. |
|---|
А в 1915 году XI-й Пироговский съезд русских врачей принял следующую резолюцию:
|
Алкоголь не может быть отнесён к питательным средствам, |
|---|
Но при всей очевидной непригодности этого опасного химического вещества для внутреннего употребления, оно является главным ингредиентом разнообразных наркотических смесей, предлагаемых населению в качестве «напитков».
Пиво, вино, шампанское, водка, коньяк — вот далеко не полный перечень ядовитых наркотических веществ, которые в нашей стране выставляются на прилавках рядом с пищевыми продуктами. Разумеется, все эти и другие растворы этанола не могут называться напитками или пищевыми продуктами, поскольку они не питают, а повреждают все органы человеческого организма, разрушая их структуру на клеточном и молекулярном уровнях.
Постоянно используемый для пропаганды этого одурманивающего зелья термин «напиток» маскирует истинную сущность наркотической смеси и способствует утверждению в сознании программы, заставляющей человека отравлять себя.
Как видим, ложь начинается с определения, что такое алкоголь. Подобных противоречий между научными фактами и бытующими в обществе суевериями очень много и по всем другим вопросам, касающимся алкоголя. И ложь эта — огромное социальное зло, угрожающее жизни каждого из нас, прочности наших семей, будущему всего нашего народа.